在电化学和光电化学反应中,理想的催化剂在较小的过电位就能够显现出较高的电流密度。
Tafel斜率能够为探究反应机制提供重要参考,特别是在阐明反应速率决定步骤和反应路径方面。
在电化学和光电化学实验中,动力学关系一般用Butler-Volmer公式[1]来表示:
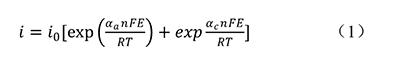
i:电流密度
i0:交换电流密度
αa:阳极电子转移系数
αc:阴极电子转移系数
n:反应中转移电子数
F:法拉第常数
E:施加电压
R:通用气体常数
T:热力学温度
在阳极高电位下,电流主要来自阳极电流,阴极电流可忽略不计,公式(1)可简化为
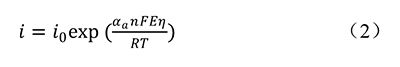
其中η为过电位,公式(2)也可被成为Tafel公式,对Tafel公式两边取对数可变为
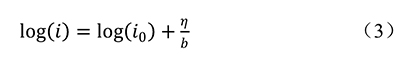
其中b表示Tafel斜率,Tafel斜率可从LSV曲线得到。 Tafel斜率还可以进一步表示为:
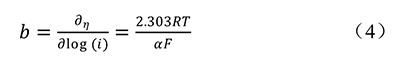
由此可知,Tafel斜率值越小,电流密度增加的越快,表明催化剂的动力学更快,催化活性越好。
如何根据实验测得的Tafel斜率来推断反应机制呢?
首先利用Tafel斜率推断出反应的速控步骤,一般光电化学反应实验需要测试工作电极HER、OER或CO2RR等性能提升效果。
测试时,要检测开路“电位-时间曲线”,当测试体系静止15 min后,且开路电位稳定时,可开始测试Tafel曲线,Tafel曲线最低点会低于开路电位,建议将开路电位减去0.1 V后的值作为参考,扫描速度值越小,试验时间越长,结果越会准确。
需要注意的是,Tafel曲线测试具有强腐蚀性,一个样品只可测一次,建议在其他无腐蚀性测试完成后,最后测试Tafel曲线,如果结果不理想,需要重新制备样品,并更换电解液再进行测试。
![图1. 经典Tafel方法在非氧化还原缓冲体系中应用原理图[2].jpg 图1. 经典Tafel方法在非氧化还原缓冲体系中应用原理图[2].jpg](/Uploads/UserFile/Image/1/20220715/62d17d111b17b.jpg)
图1. 经典Tafel方法在非氧化还原缓冲体系中应用原理图[2]
根据反应机理,图1中I1,a、I2,a分别为阴极斜率和阳极斜率,是由外推法得来的,拟合方法主要有两种:
① 手动计算
使用Origin软件安装Tafel Extrapolation插件进行计算。需要注意的是,数据拟合时要以log(i)为X轴,E为Y轴,不然得到的斜率是实际斜率的倒数;
② 自动计算
使用电化学工作站自带软件,是最方便的方法。

图2. Tafel plots[3-4]
通过LSV计算得到Tafel曲线图,可进一步揭示HER的催化动力学信息。对于HER来说,理论的Tafel斜率为120 mV/dec,40 mV/dec,30 mV/dec分别对应着Volmer-Heyrovsky步骤,Heyrovsky步骤,Tafel步骤[5]。
HER反应中Volmer-Heyrovsky机理,反应机理如下:
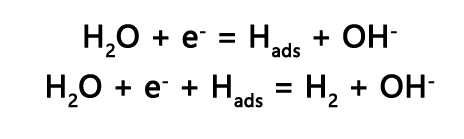
Tafel斜率较小意味着更快的动力学过程,说明催化剂可以在较低的过电势下达到所需的电流。
参考文献
[1] Stephan Enthaler*, Jan von Langermann*, Thomas Schmidt*. Carbon Dioxide and Formic Acid-the Couple for Environmental-Friendly Hydrogen Storage? [J]. Energy Environmental Science, 2010, 3, 1207.
[2] 秦越强,左勇,申淼. FLiNaK-CrF3/CrF2氧化还原缓冲熔盐体系对316L不锈钢耐蚀性能的影响[J].中国腐蚀与防护学报, 2020, 40(02):182.
[3] Ya Zhang, Lang Hu, Yongcai Zhang*, et.al. NIR Photothermal-Enhanced Electrocatalytic and Photoelectrocatalytic Hydrogen Evolution by Polyaniline/SnS2 Nanocomposites[J]. ACS Applied Nano Materials, 2022, 5: 391.
[4] Priti Sharma, Debdyuti Mukherjee, Yoel Sasson*, et. al. Pd doped carbon nitride (Pd-g-C3N4): an efficient photocatalyst for hydrogenation via an Al-H2O system and an electrocatalyst towards overall water splitting[J]. Green Chemistry, 2022, DOI: 10.1039/d2gc00801g.
[5] Guoqiang Zhao, Kun Rui, Wenping Sun*, et. al. Heterostructures for electrochemical hydrogen evolution reaction: a review [J]. Advanced Functional Materials, 2018, 28(43): 1803291.